本篇目录:
- 1、Fe+H2O(g)=高温=Fe3O4+H2的配平过程
- 2、氧化铁化学式及过程
- 3、求Fe与H2O2的反应方程式,以及一些与双氧水有关的化学方程式
- 4、单质铁在空气中被氧化的过程,要求详细分析~
- 5、fe(oh)2+o2+h2o的详细过程(中间过程)?
Fe+H2O(g)=高温=Fe3O4+H2的配平过程
这里产物三个铁共升8价,而水中氢原子共降2价变成氢气。
例如:配平Fe2O3+CO――Fe+CO2。
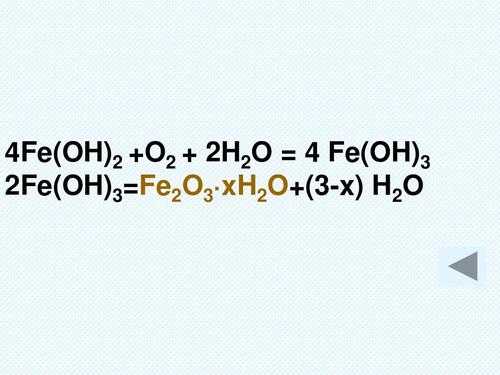
Fe+4H2O(g)=高温=Fe3O4+4H2↑6归一法找到化学方程式中关键的化学式,定其化学式前计量数为1,然后根据关键化学式去配平其他化学式前的化学计量数。
然后依然从化合价升降的最小公倍数配平MnCl从Mn守恒配平KMnO4,由K守恒配平KCl 从Cl守恒配平HCl。
根据求得的化学式的化学计量数,再找出其他化学式的化学计量数,直至配平。
氧化铁化学式及过程
1、化学式:2Al+Fe2O3=△=Al2O3+2Fe。碳还原性;氧化铁可以与碳混合后加热,铁和二氧化碳提取出来。化学式:3C+2Fe2O3=高温=3CO2↑+4Fe。高温下会分解成四氧化三铁和氧气。
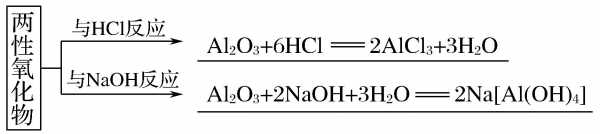
2、氧化铁的化学式写为Fe2O3。氧化铁是红色或深红色无定形粉末。相对密度5~25,熔点1565℃(同时分解)。不溶于水,溶于盐酸和硫酸,微溶于硝酸。遮盖力和着色力都很强,无油渗性和水渗性。
3、氧化铁与稀盐酸反应的离子方程式为Fe2O3+6HCl→2FeCl3+3H2O 氧化铁与稀盐酸反应的基本原理 氧化铁是一种化合物,化学式为Fe2O3。稀盐酸是一种酸性溶液,主要成分为盐酸(HCl)。
求Fe与H2O2的反应方程式,以及一些与双氧水有关的化学方程式
答案:双氧水和铁会产生氧气和水,化学方程式为:2H2O2 + Fe → 2H2O + O2 + Fe 例题2:双氧水和铁反应时,生成了多少升的氧气,如果反应中使用了100克双氧水和50克铁?答案:首先,我们需要将质量转换成摩尔数。
反应方程式如下: Fe + H2O2 - Fe2+ + H2O + O2 对于这个反应,你可以进行以下实验:材料:细铁粉,双氧水,试管,滴管 步骤:在试管中加入适量的细铁粉。用滴管向试管中滴加适量的双氧水。
Fe + HO+ 6H=2Fe +2HO +2H刚开始的反应应该是先生成二价铁离子和氢气,接着直接被氧化成三价铁离子。
双氧水可以还原三价铁但同时双氧水又可以氧化二价铁,反应的净结果是三价铁未变。
Fe2+ (亚铁离子)+ H2O2(双氧水) + 2H+(氢离子) = 2Fe3+(铁离子) + 2H2O(水)【注意:右边要加氢离子】Fe2+ 亚铁离子一般呈浅绿色,有较强的还原性,能与许多氧化剂反应,如氯气,氧气等。
单质铁在空气中被氧化的过程,要求详细分析~
铁在空气中会发生缓慢氧化,生成铁锈,其主要成分比较复杂,通常简略用Fe2O3·xH2O表示。所以铁锈可以说是混合物。
铁被氧化,一般只有这两种情形:一是在氧气中剧烈燃烧,直接生成Fe3O4(不生成Fe2O3);二是铁在空气中的氧气和水的作用下,生成氧化铁水合物Fe2O3·xH2O。
是铁单质经过在空气中不断被氧气、水共同作用而被氧化,先形成氢氧化亚铁,然后进一步氧化,变成氢氧化铁,最后变成氧化铁。
fe(oh)2+o2+h2o的详细过程(中间过程)?
1、滴入氢氧化钠溶液到硫酸亚铁溶液中有白色絮状沉淀生成。白色沉淀放置一段时间,振荡后迅速变成灰绿色,最后变成红褐色。
2、氢氧化亚铁和氧气反应的现象是变成红棕色。氢氧化亚铁在常温常压下为白色固体,但极易被氧化为 Fe(OH)3,故多呈红褐色。氧化亚铁属于六方晶系,晶格常数a0=0.3258nm,c0=0.4605nm。在空气中易被氧化变为红棕色。
3、Fe(OH)3+H2O2==2Fe(OH)2+O2(g)+2H2O;当然生成的氧气继续把氢氧化亚铁迅速氧化:4Fe(OH)2+O2+2H2O==4Fe(OH)3;所以不会出现体系颜色先由黄变白,再变黄,再变白...这样往复变化的现象。
4、方程式:4Fe(OH) + O + 2HO === 4Fe(OH)氢氧化亚铁不稳定,被空气中的氧气和水氧化,生成氢氧化铁。顺便说下变化过程中的颜色变化:原本的白色沉淀迅速变成灰绿色最终变成了红褐色。
5、找到化合价变化的原子,画出双线桥,标出得失电子数; 根据得失电子守恒:氧化剂和还原剂得失电子总数相等,化合价升高总数==化合价降低总数,标系数(最小公倍数法)。不涉及化合价变化的原子根据原子守恒配平。
6、在这个分解反应中,氢氧化亚铁(Fe(OH)2)在受热的作用下分解为氧气(O2)和铁(III)氧化物(Fe2O3)。这个反应过程实际上是吸热反应,因为它需要吸收外部能量来克服化学键的能量,使得反应发生。
到此,以上就是小编对于fe2o3·xh2o是什么的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏