本篇目录:
请问格式试剂的原理是什么?
格氏试剂是一种活泼的有机合成试剂,能够发生:偶连、加成、取代等多种类型反应,在有机合成中具有较高应用价值。
格氏反应的原理是:亲核加成。格氏的烷基部分带有强的负电性,是一个强亲核试剂。 当与含羰基的有机化合物相遇时, 格氏试剂的烷基部分很容易加成道羰基的C上。
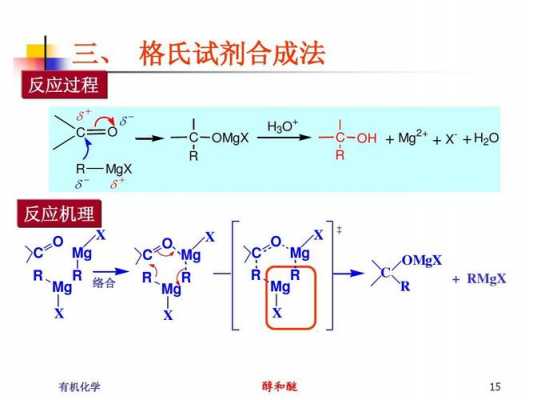
根据查询中国工业网得知,在制备格氏试剂时,生成的试剂将与卤化物发生Wurtz反应进行偶联。当格氏反应之中无水无氧条件不严格时,会与水反应生成烷烃,与氧反应生成醇盐。
格氏试剂在酵的稀溶液中以单体形式存在,并与两分子醚络合,浓溶液中以二聚体存在。原理由于镁原子直接和碳链相连,极化作用的结果是使邻近镁原子的那个碳原子呈负电性,使得这根C-Mg键极具反应活性。
格林尼亚试剂简称“格氏试剂”。格氏试剂是共价化合物,镁原子直接与碳相连形成极性共价键,碳为负电性端,因此格氏试剂是极强的路易斯碱,能从水及其它路易斯酸中夺取质子。
格氏试剂的反应机理
格氏试剂一般有两种,1:氯苯类(氯化苄)在乙醚(四氢呋喃)下和镁反应,2:溴代环戊烷在乙醚(四氢呋喃)下和镁(锌)反应。由于格式试剂本身有较强的的活性,因而格式试剂与醛、酮均可发生明显的化学反应。

格氏反应的原理是:亲核加成。格氏的烷基部分带有强的负电性,是一个强亲核试剂。 当与含羰基的有机化合物相遇时, 格氏试剂的烷基部分很容易加成道羰基的C上。
格氏试剂的基本反应通常是将格氏试剂,由氯化钠或硫酸钠溶液和低碳酸钠溶液组成,加入液体样品中,加入弱的碱性溶液,室温下反应成一种萃取液。
丙醛和格式试剂反应方程式怎么写
1、×crh5mjbr反应,然后再加水的反应方程式,这个我也不会了。
2、丙醛能发生银镜反应斐林反应。丙醛银镜反应(即与氢氧化二氨合银反应)方程式为:CH3CH2CHO+2Ag(NH3)=2Ag+3NH3+CH3CH2COONH4+H2O。
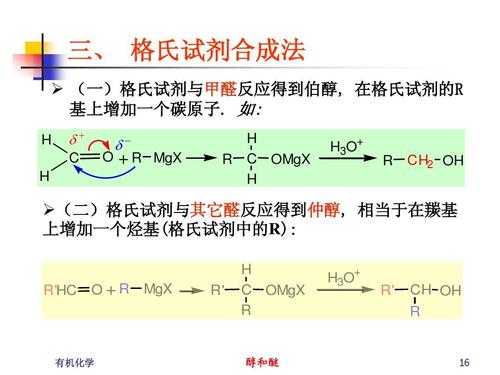
3、nC6H5OH+nHCHO→-[(C6H3OH)-CH2-]n-+nH2O。苯酚和丙醛反应方程式如上,苯酚一种具有特殊气味的无色针状晶体,有毒,丙醛,是一种有机化合物,化学式为C?H?O,为无色透明液体。
4、丙醛和氯气反应的化学方程式:CH3CH=CH2+Cl2==CH3CHClCH2Cl。C6H6 + Cl2 --- C6H5Cl + HCl。CH3CH2CHO + 2Ag(NH3)2OH --- CH3COONH4 + 2Ag + 3NH3 + H2O。
5、三种物质中分别加入银氨溶液,能生成光亮银镜的是丙醛,丙醛与银氨溶液在水浴加热条件下反应生成丙酸铵、水、银、氨气。不反应的则是丙酮和丙酸。
格氏试剂的基本反应
1、格氏试剂的基本反应是RMgX+ROH=RH+ROMgX,格氏试剂是有机合成中非常重要的试剂之一,一直在有机合成和药物合成中发挥着举足轻重的作用。
2、格氏试剂的反应机理如下:格氏试剂可以与二氧化碳或氧气发生亲核加成反应生成增加一个碳的羧酸或同碳数的过氧化合物。格氏试剂与二氧化碳的加成反应在有机合成中也有着重要的意义。
3、格氏试剂的反应方程式:CH3CH2Cl+Mg-CH3CH2MgCl(格式试剂)。格氏试剂可以与二氧化碳或氧气发生亲核加成反应,生成增加一个碳的羧酸或同碳数的过氧化合物。
格氏试剂与卤代烃反应得到什么?
格氏试剂可与各种不饱和键发生加成反应,生成不同类型的产物。反应时,格氏试剂中的C—Mg键断裂,烃基加到不饱和键中电子云密度小的原子上,镁原子加到电子云密度大的原子上。
格氏试剂可以与二氧化碳或氧气发生亲核加成反应生成增加一个碳的羧酸或同碳数的过氧化合物。格氏试剂与二氧化碳的加成反应在有机合成中也有着重要的意义。
与卤代烃反应 格氏试剂与格氏试剂反应,产物经水解生成烃。Ar-CH2X+RMgX→→Ar-CH2-R 与羰基化合物反应 格氏试剂非常容易与羰基化合物进行加成反应,所得到的加成产物经水解可形成醇。
利用伯卤代烃制成格氏试剂后,再同醛反应后水解就可以得到2-丁醇。
卤代烃与Mg在无水乙醚中的格氏试剂制备的活性是:溴大于氯。因为:1)C-Cl键比C-Br强。2)C-Br上的C的亲电性跟强。
首先回答可以反应。格式试剂是由金属镁和卤代烃在乙醚中反应得到。在其结构中,镁原子与碳链直接相连。相比碳原子,镁原子的电负性更弱,因而镁-碳键的成键电子偏向碳,使得碳带部分负电荷。
到此,以上就是小编对于格式试剂反应过程是什么的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏