本篇目录:
典型酸碱中和离子方程式
醋酸为弱电解质,醋酸和氢氧化钠溶液反应生成醋酸钠和水,离子方程式:CH3COOH+OH-=CH3COO-+H2O。一,详细解析 醋酸与氢氧化钠的反应应该是属于一个酸碱中和反应。在这个反应中,醋酸是一种弱酸。
醋酸与氢氧化钠反应的离子方程式为:CH3COOH+ OH-→CH3COO-+H2O。这个反应是一个酸碱中和反应,醋酸是一种有机酸,其化学式为CH3COOH,氢氧化钠是一种强碱,其化学式为NaOH。

盐酸和氨水的离子方程式是:H++NH3=NH4+。这个离子方程式表示盐酸中的氢离子(H+)和氨水中的氨分子(NH3)反应生成铵离子NH4+。这是一个典型的酸碱中和离子方程式必须遵循电荷守恒,即等号两边的电荷总数必须相等。
碳酸钠与盐酸离子方程式:CO32-+2H+→H2O+ CO2↑。碳酸钠(Na2CO3)与盐酸(HCl)的反应是一个典型的酸碱中和反应。在这个过程中,碳酸钠的碳酸根离子(CO32-)与盐酸的氢离子(H+)结合,形成水和二氧化碳。
小苏打与盐酸反应的离子方程式反应的化学方程式为:NaHCO+HCl→ NaCl+ HO+ CO↑。小苏打(NaHCO)与盐酸(HCl)的反应是一个典型的酸碱中和反应。
烧碱和醋酸反应的离子方程式如下:醋酸和氢氧化钠反应离子方程式:CH3COOH+OH-=CH3COO-+H2O。醋酸与氢氧化钠的反应是一个典型的酸碱中和反应。

氢氧化钠和硫酸离子方程式过程?
1、氢氧化钠和硫酸的离子方程式是:H+ + OH- = H2O。氢氧化钠(NaOH)和硫酸(H2SO4)是两种常见的化学反应物。它们的离子方程式描述了它们之间的反应过程。
2、氢氧化钠(NaOH)和硫酸(H2SO4)反应的离子方程式如下:NaOH + H2SO4 → Na+ + SO4^2- + H2O 在该反应中,氢氧化钠和硫酸发生中和反应,生成了钠离子(Na+)、硫酸根离子(SO4^2-)和水(H2O)。
3、氢氧化钠和硫酸反应的化学方程式如下:2NaOH + H2SO4 → Na2SO4 + 2H2O 该反应产生了硫酸钠和水。其中,氢氧化钠(NaOH)是碱性物质,硫酸(H2SO4)是酸性物质。
4、离子方程式 表示,其它难溶的物质.难电离的物质、气体、氧化物,水等仍用化学式表示。
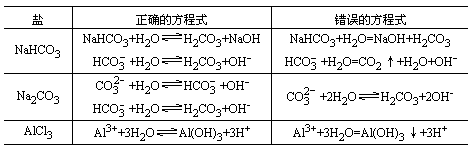
5、=Na2SO4+2H2O 氢氧化钠和硫酸的反应属于酸碱中和反应 定义:酸和碱作用生成盐和水的反应叫中和反应,是化学反应中复分解反应的一种。实质:酸电离的氢离子和碱电离的氢氧根离子相互作用生成水的过程。
离子反应方程式
1、如在FeCl2溶液中通入Cl2,其离子方程式不能写成: Fe2++Cl2=Fe3++2Cl-,因反应前后电荷不守恒,应写成:2Fe2++Cl2=Fe3++2Cl-。不能因约简离子方程式中局部系数而破坏整体的关系量。
2、离子反应方程式:碱与酸酐的反应 多酸的酸酐与碱反应,酸酐少量生成正盐,酸酐过量生成酸式盐。
3、离子反应方程式如下:离子方程式,即用实际参加反应的离子符号表示离子反应的式子。是指可溶性物质可拆的反应。离子方程式不仅表示一定物质间的某个反应,而且表示同一类型的离子反应。
4、离子方程式中量不同而面目不同多有存在,百变不离其宗,抓住基本方法,书写就能快速准确:酸式盐与碱反应,少量物质定为1(阴阳离子参加反应,计量系数必须符合组成关系),多量物质需要多少写多少。
5、离子方程式:OH+CA2++2HCO3=CACO3沉淀+H20+(CO3)2- (2)NaHSO4溶液。现象:生成气体并且有白色沉淀 离子方程式:CA2+ +2H+ +2HCO3- +(SO4)2-=2H2O+CASO4沉淀+2CO2(气体)(3)Na2Co3溶液。
6、先写方程式:Ba(OH)+2HCl=BaCl+2HO。然后拆开:Ba+2OH+2H+2Cl=Ba+2Cl+2HO。
到此,以上就是小编对于用离子方程表征中和反应的本质的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏