本篇目录:
GMP认证的过程是什么?
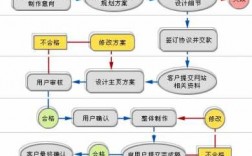
GMP认证的流程:企业到省局受理大厅提交认证申请和申报材料 。药品安全监管处对申报材料形式审查 (5个工作日) 。中心对申报材料进行技术审查 (10个工作日) 。
GMP认证之药品生产企业组织机构图 5 药品生产企业负责人、部门负责人简历;依法经过资格认定的药学及相关专业技术人员、工程技术人员、技术工人登记表,并标明所在部门及岗位;高、中、初级技术人员占全体员工的比例情况表。
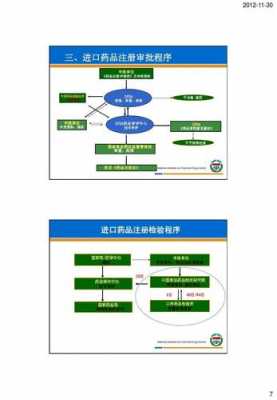
兽药gmp认证流程如下:到当地畜牧局询问GMP认证的具体要求。按要求逐步整理,直到各项达标。向畜牧局递交GMP认证申请。相关人员到工作地点现场检查。
药品生产过程验证的按验证对象分类为哪些
工艺验证 在特殊过程中,工艺验证是至关重要的一环。它包括对设备、操作手法、工艺参数等进行确认,以确保这些要素能够满足特殊过程的要求。
成分分析 药物成分的分析是药物研究的基础。需要通过各种现代分析技术,如色谱、质谱、核磁共振等,对药物中的各种化学成分进行定性和定量分析,确定药物的组成和结构,为后续的质量控制和生产提供基础数据。
一种新药上市要经过4期临床实验。就是将药物“临床试验”的过程分为四个周期,即I期一IV期。I—III期临床研究是新药上市前的必备研究,IV期是新药上市后应用研究阶段。

药物分析(习惯上称为药品检验)是运用化学的、物理学的、生物学的以及微生物学的方法和技术来研究化学结构已经明确的合成药物或天然药物及其制剂质量的一门学科。
GMP认证很重要,对药厂来说,GMP是英文Good Manufacturing Practice 的缩写,中文的意思是“良好作业规范”,或是“优良制造标准”,是一种特别注重在生产过程中实施对产品质量与卫生安全的自主性管理制度。
一种药品上市要经过多少期临床验证,分别验证是哪些内容
分为4期。I期临床试验。其目的是研究人体对药物的耐受程度,并通过药物代谢动力学研究,了解药物在人体内的吸收、分布、消除的规律,为制定给药方案提供依据,以便进一步进行治疗试验。II期临床试验。
临床试验分为Ⅰ、Ⅱ、Ⅲ、Ⅳ期。新药在批准上市前,申请新药注册应当完成Ⅰ、Ⅱ、Ⅲ期临床试验。
III期临床试验:治疗作用确证阶段。其目的是进一步验证药物对目标适应症患者的治疗作用和安全性,评价利益与风险关系,最终为药物注册申请的审查提供充分的依据。试验一般应为具有足够样本量的随机盲法对照试验。
药品的临床试验为分4期。其中3期的临床试验要在药品正式上市之前完成。而4期临床试验,是在上市之后再进行的。临床试验主要用于研究药品的药效与风险,为上市审评时提供可靠的数据支撑。
期临床试验:通常为期数月,旨在测试药物的安全性,这一关比较好过,通过率高达70%。2期临床试验:2期临床试验又可以分为两个阶段,2a和2b。2a阶段仅仅是在一个很小的范围内测试一下药物的有效剂量。
到此,以上就是小编对于药品验证的定义的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏