本篇目录:
- 1、如何制取稀盐酸?
- 2、往na[al(oh)]4溶液中逐滴加入稀盐酸,实验过程的现象是?有关的化学方程...
- 3、此图中实验步骤三加足量稀盐酸的目的是什么,是为了将其中某种物质从溶液...
- 4、大理石与稀盐酸反应制取二氧化碳的实验步骤是什么
- 5、稀盐酸溶液的配置?
- 6、向大理石表面滴加稀盐酸的现象
如何制取稀盐酸?
1、实验室制取氯化氢有三种方法:二氧化氯法、重水水解法、氯化钠与浓硫酸供热法。三种方法具体如下:盐酸主要由氯化氢溶于水来制备。而氯化氢可以通过氯气与二氧化硫在水溶液中作用来制备。
2、将水注入到第二个试管 将氯气注入到第二个试管。立马走到通风口,立马盖上盖子。把第二个盛有的氯气和水的试管摇1分钟,即可制出少量盐酸。
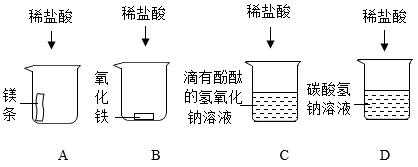
3、要看你用名都为多少的稀盐酸了 一般用的稀盐酸浓度是25%。如果称量的方式进行配制。
4、Mg(OH)2+2HCl=MgCl2+2H2O。实验室制取二氧化碳:CaCO3+2HCl=CaCl2+H2O+CO2↑。与铁,镁等金属反应生成化学实验需要的少量氢气Fe+2HCl=FeCl2+H2↑,Mg+2HCl=MgCl2+H2↑。
5、NaCl+2H2O==2NaOH+Cl2+H2(电解),Cl2+H2==2HCl(点燃),将氯化氢溶于水,形成盐酸,2NaOH+CO2==Na2CO3+H2O (CO2适量)。在通常情况下,氯化钠是晶体。
往na[al(oh)]4溶液中逐滴加入稀盐酸,实验过程的现象是?有关的化学方程...
1、往NaAl(OH)4溶液中逐滴加入稀盐酸,先产生白色胶状沉淀,稀盐酸过量后,白色沉淀逐渐溶解。
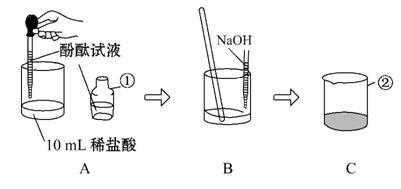
2、第一个实验,Al(OH)4多HCl与他反应生成沉淀,然后H过量生成沉淀。
3、稀盐酸和氢氧化钠反应现象是向红色溶液中逐滴滴加稀盐酸溶液,红色溶液逐渐褪色,最后变成无色透明的溶液后,继续加稀盐酸溶液,溶液不变色,仍是无色透明。氢氧化钠和盐酸反应化学方程式: HCl+NaOH=NaCl+H2O。
4、碳酸钠与稀盐酸反应的化学方程式如下:当盐酸少量或等量时:HCl+Na2CO3=NaHCO3+NaCl;当盐酸为过量时:2HCl+Na2CO3=2NaCl+CO2↑+H2O。若在碳酸钠中不断滴入稀盐酸,现象是一开始无气泡产生,一段时间后溶液产生气泡。
此图中实验步骤三加足量稀盐酸的目的是什么,是为了将其中某种物质从溶液...
1、溶液:一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物 溶液的组成:溶剂和溶质。
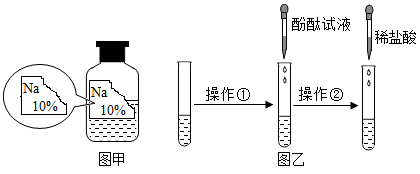
2、填空题: 实验室有三瓶没有标签的液体,分别是氢氧化钠溶液、硫酸铜溶液和稀盐酸,不用其他试剂,设计一 个实验方案进行鉴别,并完成实验报告。
3、C.真黄金和假黄金(铜锌合金):滴加稀盐酸或灼烧D.氧气和二氧化碳:滴加酚酞溶液或将燃着的木条伸入航天探测发现:金星是一个被浓密大气层包围的固体球,大气层的成分之一是C2O3实验证明其化学性质与CO相似。
大理石与稀盐酸反应制取二氧化碳的实验步骤是什么
1、实验室制取二氧化碳的方法:大理石与稀盐酸反应制取。
2、大理石与稀盐酸反应制取。(1)实验器材:试管、酒精灯、试管夹、镊子、药匙、量筒、纸槽、集气瓶、毛玻璃片、稀盐酸。(2)实验步骤:取一支试管,用镊子夹取一小块大理石放入试管口。
3、实验室制取二氧化碳的操作步骤如下:选择合适的试剂并加入到启普发生器中。在选择试剂时,需要考虑反应速度、成本、产气效率等因素。
4、反应原理 CaCO3+2HCl=CaCl2+H2O+CO2↑ 实验步骤 “查”:检查装置的气密性。“装”:从锥形瓶口装大理石,塞紧塞子。“加”:从长颈漏斗(或分液漏斗)加入稀盐酸。“收”:收集气体。
5、实验步骤:连接装置。检查气密性。在锥形瓶中装入大理石(或石灰石)从长颈漏斗中加入稀盐酸。收集气体。注意:制取二氧化碳时,不能将稀盐酸换成浓盐酸。
6、二氧化碳制取方法如下:碳酸盐与较强酸的反应(本质上是碳酸根/碳酸氢根与强酸的反应):以碳酸钠和盐酸为例:Na2CO3+2HCl==2NaCl+H2O+CO2↑/NaHCO3+HCl==NaCl+H2O+CO2↑。
稀盐酸溶液的配置?
配制盐酸溶液的方法:配制0.02mol/LHCl溶液:量取8毫升盐酸,缓慢注入1000ml水。0.1mol/LHCl溶液:量取9毫升盐酸,缓慢注入1000ml水。0.2mol/LHCl溶液:量取18毫升盐酸,缓慢注入1000ml水。
用17mL的浓盐酸加100mL的水来配制。浓盐酸的摩尔浓度是 12 mol/L.假设配制100 mL的0.5mol/L的稀盐酸,算法如下:所需的HCl的物质的量 = 0.1 L * 0.5 mol/L = 0.05mol。
配制:0.01mol/LHCl溶液:量取0.9毫升盐酸,缓慢注入1000ml水。
搅拌均匀,即可得到0、6 mol/L的盐酸溶液。需要注意的是,在配制盐酸溶液时,应佩戴防护眼镜和手套,避免溅射造成伤害。同时,在配制过程中应保持通风良好,以避免吸入盐酸蒸气对身体造成伤害。
注入1000mL水 摇匀,使浓盐酸与水混合 密闭储存 完成配置 要配制1升0.1mol/L的稀盐酸,需要12mol/L的浓盐酸的体积是,1000×0.1/12=3毫升。即量取浓盐酸3毫升加水稀释到一升溶液即可。
药典稀盐酸溶液配置:37-38%的浓盐酸的物质的量的浓度为12mol/L,要酸5mol/L的稀盐酸只要取浓盐酸0.21ml加入适量蒸馏水中,边加边搅拌,用蒸馏水稀释至1000ml,摇匀。即得1000ml浓度为5mol/L的稀盐酸。
向大理石表面滴加稀盐酸的现象
1、由于大理石的主要成分是碳酸钙,而稀盐酸能够与碳酸钙反应生成氯化钙、水和二氧化碳,所以该过程出现的现象是大理石表面有气泡产生。
2、因为大理石的主要成分是碳酸钙,所以与盐酸反应后会生成二氧化碳。如果将点燃的木条放在试管口得出现象:放在试管口不会灭,因为二氧化碳的密度比空气重。
3、加热条件下,少量大理石与稀盐酸反应的现象是:剧烈反应,试管中迅速产生气泡,大理石体积缩小,溶液始终为无色。
到此,以上就是小编对于实验用稀盐酸怎么配置的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏