本篇目录:
- 1、为什么理想气体节流膨胀ΔU=0
- 2、绝热过程都是等焓过程吗
- 3、物化,在什么情况下焓变为0?比如可逆膨胀这种
- 4、绝热节流的实质是什么?只知道是等焓、熵增过程,但详细的能量怎么损失...
- 5、理想气体绝热节流后,其状态参数熵,焓,温度各自怎么变化
- 6、等焓状态什么意思?
为什么理想气体节流膨胀ΔU=0
节流膨胀:较高压力下的流体(气或液)经多孔塞(或节流阀)向较低压力方向绝热膨胀过程。根据热力学原理,在焦耳-汤姆逊实验中系统对环境做功-W=p2V2-p1V1,V1及V2分别为始态和终态的体积。
所谓自由膨胀就是向真空膨胀,不克服外力,自由膨胀过程不做功w=0。又知恒温膨胀,内能不变,△u=0(理想气体内能仅是温度的函数)。故q=0,这说明理想气体恒温自由膨胀就是绝热自由膨胀。
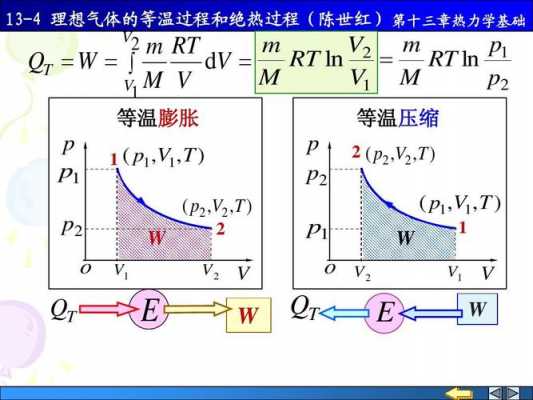
(2)理想气体节流膨胀过程:△H=0,温度不变于是△U=0。同时是绝热可逆过程,△S=0。(3)实际气体节流膨胀:△H=0,产生致冷或致热效应pv变化,由定义△U不等于零。(4)绝热可逆过程△S=0。
绝热过程都是等焓过程吗
1、气体绝热节流,可以肯定的是:焓值不变,压力下降,熵增大。绝热节流前后工质的温度会发生变化,即节流的温度效应,温度可以升高、可以降低、也可以不变(对于理想气体前后温度肯定是不变)。
2、是。根据查询作业帮显示,可逆的绝热过程是等熵过程。等熵过程的对立面是等温过程,在等温过程中,最大限度的热量被转移到了外界,使得系统温度恒定如常。
3、不一定,绝热过程不一定是等熵过程。比如气体对真空的自由膨胀过程是不可逆过程,熵增。
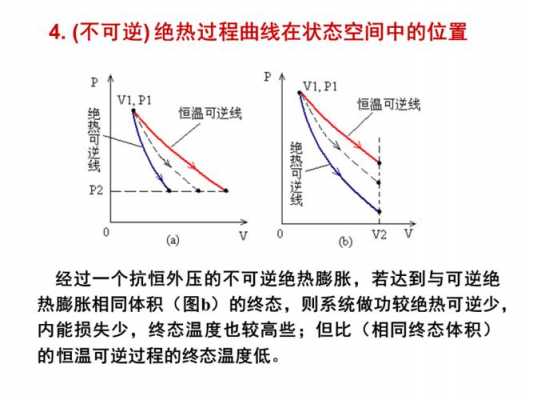
4、在绝热过程中,系统内部的能量不会改变,因为没有热量进出系统,因此绝热过程是一个等熵过程(isentropic process)。而其他领域中的绝热可能指的是不透过热量、声波或电场等的物理过程。
5、在绝热的条件下,向空气加入水分以增加其含湿量,叫绝热加湿。因为是绝热的,水分蒸发所吸收的潜热完全来自空气自身。加湿以后空气温度将降低,所以这种过程又称为蒸发冷却过程。
物化,在什么情况下焓变为0?比如可逆膨胀这种
1、(2)理想气体节流膨胀过程:△H=0,温度不变于是△U=0。同时是绝热可逆过程,△S=0 (3)实际气体节流膨胀:△H=0,产生致冷或致热效应pv变化,由定义△U不等于零 (4)绝热可逆过程△S=0。
2、也就是说,△H在非等压情况下不等于△Q。所以非等压下的焓变的物理意义不是系统放出或吸收的热。

3、由吉布斯函数判据,恒温恒压非体积功为零时吉布斯函数变化小于等于零,相变显然满足恒温恒压无非体积功,又是可逆相变,所以它等零。吉布斯自由能改变量。表明状态函数G是体系所具有的在等温等压下做非体积功的能力。
绝热节流的实质是什么?只知道是等焓、熵增过程,但详细的能量怎么损失...
节流过程是指流体流动时由于通道截面突然缩小(如孔板、阀门等)而使压力降低的热力过程。
由于节流现象时间很短,系统与外界的能量传递可以忽略不计,因此节流是绝热过程。由于系统没有能量的输入,所以节流前、后的焓值不变,即等焓过程。
绝热节流的四个特点是:1)节流过程严重不可逆,是典型的不可逆过程。
【答案】:错误绝热节流前后焓值相等,但能量的品质下降了。因为绝热节流是不可逆过程,有熵增,即无效能增加,故能量品质下降。
V1及V2分别为始态和终态的体积。Q=0,故ΔU=-(p2V2-p1V1);U2+p2V2=U1+p1V1;即H2=H1。所以焦耳-汤姆孙实验(简称焦汤实验)的热力学实质是焓不改变,或者说它是一个等焓过程。
理想气体绝热节流后,其状态参数熵,焓,温度各自怎么变化
压力降低 比容(单位质量的体积)增大 焓不变 内能不变 熵增大 如有不明欢迎追问。
饱和温度随压力的降低而降低。对于理想气体,是温度的单值函数。所以绝热节流后焓值不变,温度也不变。对于实际气体,焓是温度和压力的函数,经过绝热节流后,温度降低、升高和不变3种情况都可能出现。
焓:热力学中表示物质系统能量的一个状态函数,常用符号H表示。数值上等于系统的内能U加上压强p和体积V的乘积,即H=U+pV。焓的变化是系统在等压可逆过程中所吸收的热量的度量。
绝热又不对外界做功,根据稳定流动能量方程,可得节流前后Δh=0,即h1=h2。绝热节流前后工质的温度会发生变化,即节流的温度效应,温度可以升高、可以降低、也可以不变。但对于理想气体前后温度肯定是不变喽。
对于理想气体等温膨胀这一可逆过程dU=0。所以dQ=dU+PdV=PdV于是:上式就是理想气体向真空自由膨胀,初末两态的熵变。因为V2V1。,所以S2-S10,这说明:在不可逆绝热过程中熵增加。
首先绝热节流过程并不一定温度就是降低,这要看流体的种类,有节流冷效应和热效应等。另外在绝热节流过程中比体积是增大的,H=U+PV,你如果非要从本质入手很难分析,这其中本身有一定的近似因素。
等焓状态什么意思?
1、焓,H;或 比焓,h.在一个等焓过程没有热调动到(或从)周围和在(或)周围完成的没有工作。通常将有在压力和温度上的重大的变化在过程期间。节流过程 是一个等焓过程的一个好例子。考虑举一个泄压阀或安全阀在压力容器。
2、焓值 热力学中表示物质系统能量的一个状态函数,常用符号H表示。数值上等于系统的内能U加上压强p和体积V的乘积,即H=U+pV。焓的变化是系统在等压可逆过程中所吸收的热量的度量。
3、焓指能量,熵指混乱度。焓的物理意义是体系中热力学能再附加上PV这部分能量的一种能量,H=U+pV,熵的物理意义是体系的混乱程度,定义式:dS=dQ/T。
4、等熵态、等温态、等焓态:物质的不同性质 固体、液体、气体和等离子体、玻璃态、凝胶态等物质的状态可以根据不同条件下物质内部的性质划分,例如等熵态、等温态、等焓态。
5、首先,处理到室内等焓的意思是新风不承担室内负荷,也就是意味着,处理到等焓状态的新风已经是达到了室内送风点的状态参数。但是全热交换设备只是利用室内排出的冷气将新风进行冷却,然后送到室内。
6、因为热湿平衡过程中焓值没变。一个体系从状态1变化到状态2的过程中,若其焓值不变,则称之为等焓过程。而热湿平衡过程中就是得热量和失热量相等,得湿量与失湿量相等,所以热湿平衡是一个等焓过程。
到此,以上就是小编对于绝热可逆过程是一个等焓过程的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏