本篇目录:
怎么理解热力学可逆过程?什么是等温可逆,绝热可逆,可逆相变?
1、可逆过程是指热力学系统在状态变化时经历的一种理想过程。热力学系统由某一状态出发,经过某一过程到达另一状态后,如果存在另一过程,它能使系统和外界完全复原。
2、绝热可逆过程:Q=0,△U=W=-P外dV(恒外压);或△U=nCv,mdT;△H=nCp,mdT。物体的温度 等温可逆膨胀:物体的温度是恒定的,所以要吸收或者放热的,如果没有外接做功的话同样不能可逆。
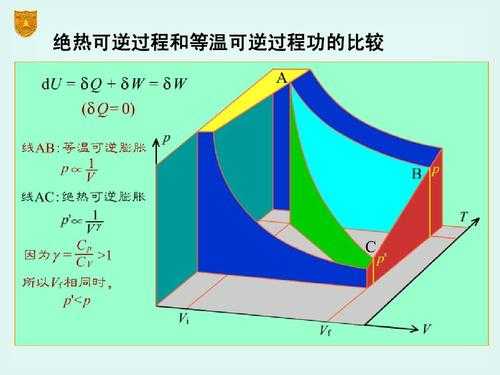
3、绝热可逆过程:Q=0,△U=W=-P外dV(恒外压) 或 △U=nCv,mdT, △H=nCp,mdT 绝热可逆膨胀:物体的温度可是要变化的。如果没有外界做功的话应该不能够可逆。
4、可逆过程是指热力学系统在状态变化时经历的一种理想过程。热力学系统由某一状态出发,经过某一过程到达另一状态后,如果存在另一过程,它能使系统和外界完全复原,即使系统回到原来状态。
5、绝热可逆过程:就是体系没有热量的散失,且该反映是可逆的过程。可逆的绝热过程是等熵过程。等熵过程的对立面是等温过程,在等温过程中,最大限度的热量被转移到了外界,使得系统温度恒定如常。
等温等压可逆相变过程为恒什么过程
1、可逆相变化过程一定是恒温恒压过程。两相之间在一定温度时的相平衡压力下发生的相变化。即发生在此温度下此物质的饱和蒸汽压下的相变,即恒温恒压条件下的物理相变。
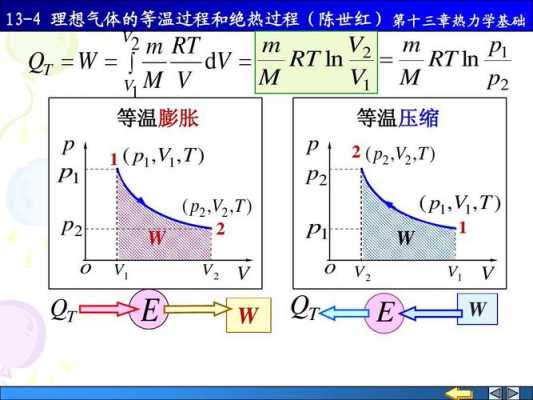
2、绝热可逆过程:Q=0,△U=W=-P外dV(恒外压);或△U=nCv,mdT;△H=nCp,mdT。物体的温度 等温可逆膨胀:物体的温度是恒定的,所以要吸收或者放热的,如果没有外接做功的话同样不能可逆。
3、绝热可逆过程:Q=0,△U=W=-P外dV(恒外压) 或 △U=nCv,mdT, △H=nCp,mdT 绝热可逆膨胀:物体的温度可是要变化的。如果没有外界做功的话应该不能够可逆。
物理化学中的可逆过程是怎么回事?
可逆过程是指热力学系统在状态变化时经历的一种理想过程。热力学系统由某一状态出发,经过某一过程到达另一状态后,如果存在另一过程,它能使系统和外界完全复原。
逆过程是在作用力与阻力相差无限小的条件下进行的。过程的速率无限缓慢。每一瞬间,系统都无限接近于平衡状态。过程中没有摩擦发生。可逆过程发生后,可以使系统沿原途径逆向进行恢复原状,而不给环境留下任何痕迹。

逆过程是在作用力与阻力相差无限小的条件下进行的。过程的速率无限缓慢。每一瞬间,系统都无限接近于平衡状态。过程中没有摩擦发生。
可逆过程指一个过程发生后,体系恢复原状态后,环境也恢复原状态。换句容易理解的话说就是,经过这么一个过程,人畜无伤,没有任何影响。并且这个过程中每个截点都是相对稳定的。在题目中已经告诉你了,等温可逆。
可逆过程:一个体系经过某过程后,体系与环境发生了变化,如果能使体系和环境都完全复原而不引起其它变化, 则称原来的过程是可逆过程。
到此,以上就是小编对于等温可逆过程g等于a的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏