本篇目录:
sp,sp2,sp3杂化的区别,怎样形成sp3杂化???
1、sp,sp2,sp3杂化的区别:中心云的构型不同。中心原子连接的原子数不同。具体如下:sp 杂化轨道所成的电子云是直线型的,中心原子连接2个原子(或孤对电子)。
2、sp2杂化形成的杂化轨道具有平面三角形特征,通常发生在分子中的π键或配位键上。而sp3杂化形成的杂化轨道具有四面体结构,通常发生在分子中的σ键或配位键上。
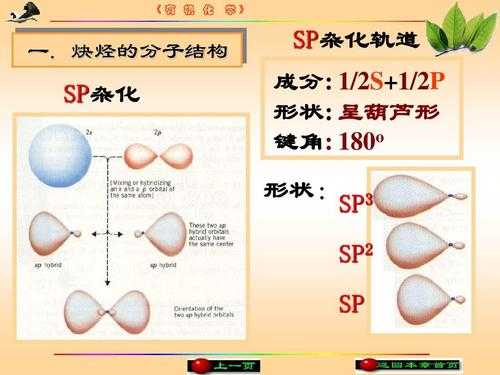
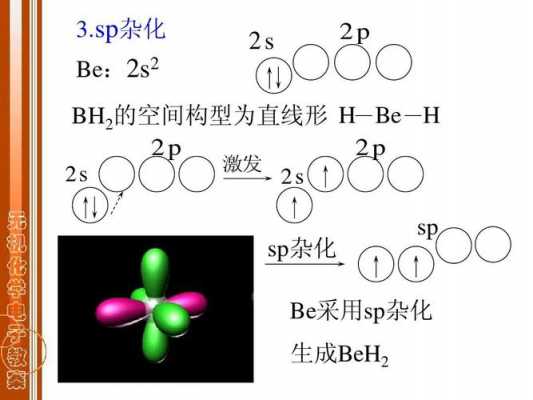
3、sp杂化同一原子内由一个ns轨道和一个np轨道发生的杂化,称为sp杂化。杂化后组成的轨道称为sp杂化轨道。sp杂化可以而且只能得到两个sp杂化轨道 例如:气态BeCl2是一个直线型的共价分子。
4、不等性,指形成的杂化轨道中有的放了孤对电子,没有和其它原子成键。如CH4是sp3等性杂化,NHH2O是sp3不等性杂化。如BF3是sp2等性杂化,SO2是sp2不等性杂化。如BeCl2是sp等性杂化,CO是sp不等性杂化。
5、sp2杂化:同一原子内由1个ns轨道和2个np轨道参与的杂化。例如,在乙烯(CH)分子中有碳碳双键(C=C),碳原子在形成乙烯分子时,每个碳原子的2s轨道与两个2p轨道发生sp2杂化,形成3个杂化轨道。
sp杂化的空间构型是怎样的?
sp杂化轨道的空间构型:(1)线性分子,中心原子为sp杂化,如乙炔。(2)平面内的分子形如乙烯的,中心原子为sp2杂化。(3)空间(正)四面体,中心原子sp3杂化,如四氯化碳。
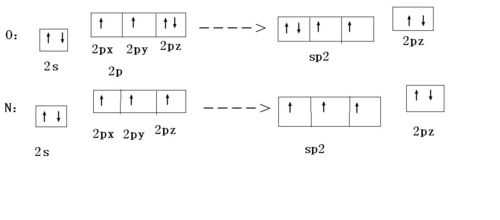
sp杂化为直线型(CO2,HC≡CH),sp2杂化为平面正三角形(BF3)sp3杂化为正四面体(甲烷),三角锥(氨),V形(H2O)dsp2杂化为正方形dsp3杂化为四方锥或三角双锥d2sp3,sp3d2杂化为正八面体。
sp3杂化空间构型是正四面体。sp3杂化,是指同一原子内由1个ns轨道和3个np轨道参与的杂化,所形成的4个杂化轨道称sp3杂化轨道。各含有1/4的s成分和3/4的p成分,杂化轨道间的夹角为109°28,空间构型为正四面体。
二氧化碳是怎么杂化的!求详解!最好有示意图!
直线型分子。sp杂化产生2个sp轨道形成sigma键,剩下两个p轨道上的单电子与氧形成pai键,而二氧化碳是直线型分子,所以,二氧化碳因为直线型分子所以是sp杂化。
二氧化碳结构的正确描述:在分子中,碳原子采用sp杂化轨道与氧原子成键。C原子的两个sp杂化轨道分别与两个O原子生成两个σ键。
是sp杂化。不一定,碳成四个σ键的时候就是sp3杂化,若要成一个π键,则需要一个p轨道,然后剩下的部分进行杂化成σ键,所以乙烯中的碳就是sp2杂化。
C原子的两个sp杂化轨道分别与一个O原子生成两个δ键。C原子上两个未参加杂化的p轨道与sp杂化轨道成直角,并且从侧面同氧原子的p轨道分别肩并肩地发生重叠,生成两个∏三中心四电子的离域键。
二氧化碳的电子式是如下图:C原子以sp杂化轨道形成δ键。分子形状为直线形。非极性分子。在CO分子中,碳原子采用sp杂化轨道与氧原子成键。C原子的两个sp杂化轨道分别与两个O原子生成两个σ键。
二氧化碳如何SP杂化
1、CO2中碳原子的杂化态是sp。这是因为CO2分子的特殊结构和碳原子周围的电子排布所决定的。CO2分子的结构可以看作是线性的,有一个碳原子和两个氧原子组成。碳原子上有两对孤对电子,氧原子上有两对非共享的孤对电子。
2、在CO2分子中,碳原子采用sp杂化轨道与 二氧化碳分子结构 [4]氧原子成键。C原子的两个sp杂化轨道分别与两个O原子生成两个σ键。
3、在CO2分子中,碳原子采用sp杂化轨道与 二氧化碳分子结构。同一原子内由1个ns 轨道和 1个 np 轨道参与的杂化称为sp杂化 ,所形成的两个杂化轨道称为SP杂化轨道。
水的杂化示意图
水的杂化示意图:水分子中的氧原子为不等性的sp3杂化。这个可以利用VSEPR理论去解释,因为VPN等于4,所以是一个sp3杂化,而且有两对孤对电子。
用杂化轨道理论解释HO分子的立体构型为V型。HO中O采取sp3杂化,四个sp3杂化轨道其中有两个被O原子的两对孤电子对占据,其余的两个sp3杂化轨道分别与两个H原子的s原子轨道形成σ键,分子构型为V形。
图1-1-2 水分子核外电子轨道示意图 由于水分子核外电子的这样一种构型,使得水分子的正负电荷中心并不重合。
到此,以上就是小编对于sp杂化什么形状的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏