本篇目录:
怎么判断化学反应放热吸热?
1、方法一:根据反应物具有的总能量与生成物具有的总能量之前的关系:反应物具有的总能量高于生成物具有的总能量,该反应为放热反应。反应物具有的总能量低于生成物具有的总能量,该反应为吸热反应。
2、化学反应是吸热还是放热可根据能量大小来判断:生成物能量大于反应物能量的,吸热反应。生成物能量小于反应物能量的,放热反应。

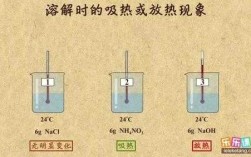
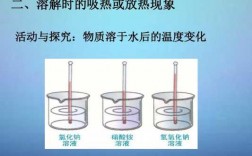
3、温度变化:观察反应过程中的温度变化是最直接的方法。如果反应过程中温度升高,那么这是一个放热反应;如果反应过程中温度降低,那么这是一个吸热反应。 反应方程式:化学反应可以通过反应方程式来描述。
4、(1)普通化学方程式只表明了化学反应中的物质变化;热化学方程式是表示反应所放出或吸收热量的化学方程式,它既表明了化学反应中的物质变化,又表明了化学反应中的能量变化。
化学反应吸热放热判定
1、(1)根据反应物具有的总能量与生成物具有的总能量之前的关系判断:反应物具有的总能量高于生成物具有的总能量,该反应为放热反应。反应物具有的总能量低于生成物具有的总能量,该反应为吸热反应。
2、温度变化:观察反应过程中的温度变化是最直接的方法。如果反应过程中温度升高,那么这是一个放热反应;如果反应过程中温度降低,那么这是一个吸热反应。 反应方程式:化学反应可以通过反应方程式来描述。

3、根据具体化学反应实例判断 (1)常见的放热反应:所有可燃物的燃烧、所有金属与酸的反应、所有中和反应、绝大多数化合反应、少数分解反应、多数置换反应、某些复分解反应。
4、化学反应是吸热还是放热可根据能量大小来判断:生成物能量大于反应物能量的,吸热反应。生成物能量小于反应物能量的,放热反应。
5、放热反应和吸热反应的判断方法有以下几种:(1)根据反应物具有的总能量与生成物具有的总能量之前的关系判断;(2)根据反应物具有的键能总和与生成物具有的键能总和的大小关系判断;(3)根据化学反应的基本类型判断。
吸热反应和放热反应定义???
1、放热反应是放出热量,是释放热量的过程,即周围气体的温度会随之升高,该物体(放热的物体)有可能升温。代表反应类型有:燃烧(氧化)、中和。放热反应的方程式:ΔH0。
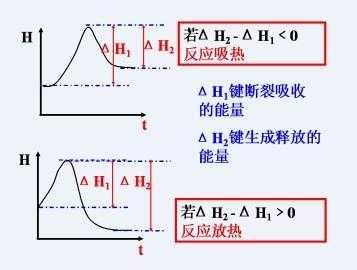
2、不是需要加热的反应都是吸热反应,燃烧大多数要“点燃”,都是放热反应。吸热反应就是在化学变化中,需要不断吸收大量热量的反应。不是所有需要使用催化剂的反应都是吸热反应。
3、吸热反应是指在过程中吸收热量的化学反应。在化学反应中,反应物总能量大于生成物总能量的反应叫做放热反应。
4、从理论上说:生成物的总能量高于反应物的总能量,那就是吸热反应,如果生成物的总能量低于反应物的总能量,就是放热反应。
5、放热反应 所有物质在氧气中的燃烧或爆炸反应,这些反应伴随发光发热,都属于放热反应。较强酸的酸酐(酸性氧化物)或较强碱的碱性氧化物和水的反应。
什么是吸热放热,初中物理
1、放热反应是放出热量,是释放热量的过程,即周围气体的温度会随之升高,该物体(放热的物体)有可能升温。代表反应类型有:燃烧(氧化)、中和。放热反应的方程式:ΔH0。
2、熔化、汽化、升华属于吸热,是温度升高发生的变化,方向为固→液→气 液化、凝固、凝华属于放热,是温度降低发生的变化.方向为气→液→固 液化分为沸腾和蒸发,升华和凝华需要温度骤变。
3、放热是这个物体温度比较高,周围物体(或环境)的温度比它低,它就对外放热,放热后温度降。汽化熔化升华是从一种状态变成另一种状态的过程,要完成这个过程,它要从周围环境吸收热量升温才能使它状态向另一种状态发生改变。
4、什么是放热和吸热 吸热现象既可以是化学变化也可以是物理变化,放热现象也是一样。 物理变化要求分子种类不发生改变,比如水的蒸发就是吸热的物理变化,而热水变凉就是放热的物理变化。
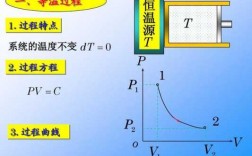
5、焓变包含于反应热包含于热效应,就相当于热效应是最大的集合。焓是与内能有关的物理量,反应在一定条件下是吸热还是放热由生成物和反应物的焓值差即焓变(△H)决定。等压条件下的 反应热等于焓变。
到此,以上就是小编对于放热过程公式的问题就介绍到这了,希望介绍的几点解答对大家有用,有任何问题和不懂的,欢迎各位老师在评论区讨论,给我留言。

 微信扫一扫打赏
微信扫一扫打赏